Атомная масса
Атомная масса (m a), которую также называют «относительной атомной массой», является массой одного атома изотопа, выраженной в атомных единицах массы, а.е.м., в которых изотоп углерод-12 имеет атомную массу, которая точно равен 12. Масса одного другого изотопа не равен целому числу результате воздействия энергии связи ядер.
Атомная масса изотопа равен целому числу приблизительно: в большинстве случаев первая цифра после запятой – это 0 или 9. Это целое число называется массовым номером и является суммой числа протонов и нейтронов в атомном ядре.
Закономерность приращение атомной массы в зависимости от массового номера такая: избыток положительного у водорода-1, становится отрицательным, пока не достигается минимум у железа-56, затем возрастает до положительных значений у тяжелых изотопов с ростом атомного номера. Это соответствует тому, что деление элементов тяжелее железо, высвобождает энергию, а расщепление элемента, легче железа требует энергии. Напротив, реакций слияния ядер: слияние элементов легче железа высвобождает энергию, слияние же элементов тяжелее железа требует дополнительной энергии.
Если речь идет химического элемента, атомная масса (также «атомная масса», «средняя атомная масса» или «атомный вес»), представленная в периодической таблице, является средней атомной массой всех стабильных изотопов данного химического элемента. Эту атомную массу используют в стохиометричних расчетах. Она обычно применяется как масса в граммах одного моля атомов элемента, что также называется молярной массой.
Термин «атомный вес» теперь постепенно вытесняется термином «относительная атомная масса». Термин «стандартная атомный вес» (который теперь использует IUPAC), касается средней относительной атомной массы элемента.
То же определение касается молекул, и в этом случае его называют молекулярной массой. Молекулярную массу соединения можно рассчитать, добавляя атомные массы элементов, составляющих ее, умноженные на коэффициенты элементов по химической формуле. Та самая масса может быть рассчитана для соединений, которые не создают молекул.
Прямое сравнение и измерение масс атомов и молекул выполняется масс-спектрометрией.
Один моль вещества равна атомной или молекулярную массу вещества, выраженную в граммах. Например, атомная масса железа равна 55,847. Поэтому один моль атомов железа весит 55,847 граммов.
До 60-х годов 20-го столетия атомную массу определяли таким образом, что изотоп кислород-16 имел атомную массу 16. Однако соотношение кислорода-17 и кислорода-18 в природном кислороде, который также использовался в расчетах атомной массы, приводило к наличию двух разных таблиц атомных масс.
Ранее химики и физики использовали две разные шкалы атомных масс. Химики использовали шкалу, основанную на том, что естественная смесь изотопов кислорода должна атомную массу 16, тогда как физики присваивали то же число 16 атомной массе наиболее распространенного изотопа кислорода (имеющего восемь протонов и восемь нейтронов). Унифицированная шкала основана на углерода-12, 12 C, что соответствует потребности физиков в шкале, основанной на чистом изотопе, и за числами стоит близко к шкалы химиков.
Атомная масса изотопа равен целому числу приблизительно: в большинстве случаев первая цифра после запятой – это 0 или 9. Это целое число называется массовым номером и является суммой числа протонов и нейтронов в атомном ядре.
Закономерность приращение атомной массы в зависимости от массового номера такая: избыток положительного у водорода-1, становится отрицательным, пока не достигается минимум у железа-56, затем возрастает до положительных значений у тяжелых изотопов с ростом атомного номера. Это соответствует тому, что деление элементов тяжелее железо, высвобождает энергию, а расщепление элемента, легче железа требует энергии. Напротив, реакций слияния ядер: слияние элементов легче железа высвобождает энергию, слияние же элементов тяжелее железа требует дополнительной энергии.
Если речь идет химического элемента, атомная масса (также «атомная масса», «средняя атомная масса» или «атомный вес»), представленная в периодической таблице, является средней атомной массой всех стабильных изотопов данного химического элемента. Эту атомную массу используют в стохиометричних расчетах. Она обычно применяется как масса в граммах одного моля атомов элемента, что также называется молярной массой.
Термин «атомный вес» теперь постепенно вытесняется термином «относительная атомная масса». Термин «стандартная атомный вес» (который теперь использует IUPAC), касается средней относительной атомной массы элемента.
То же определение касается молекул, и в этом случае его называют молекулярной массой. Молекулярную массу соединения можно рассчитать, добавляя атомные массы элементов, составляющих ее, умноженные на коэффициенты элементов по химической формуле. Та самая масса может быть рассчитана для соединений, которые не создают молекул.
Прямое сравнение и измерение масс атомов и молекул выполняется масс-спектрометрией.
Один моль вещества равна атомной или молекулярную массу вещества, выраженную в граммах. Например, атомная масса железа равна 55,847. Поэтому один моль атомов железа весит 55,847 граммов.
До 60-х годов 20-го столетия атомную массу определяли таким образом, что изотоп кислород-16 имел атомную массу 16. Однако соотношение кислорода-17 и кислорода-18 в природном кислороде, который также использовался в расчетах атомной массы, приводило к наличию двух разных таблиц атомных масс.
Ранее химики и физики использовали две разные шкалы атомных масс. Химики использовали шкалу, основанную на том, что естественная смесь изотопов кислорода должна атомную массу 16, тогда как физики присваивали то же число 16 атомной массе наиболее распространенного изотопа кислорода (имеющего восемь протонов и восемь нейтронов). Унифицированная шкала основана на углерода-12, 12 C, что соответствует потребности физиков в шкале, основанной на чистом изотопе, и за числами стоит близко к шкалы химиков.
 Просмотров: 4019
Просмотров: 4019
 Дата: 24-02-2011
Дата: 24-02-2011
Изотопы
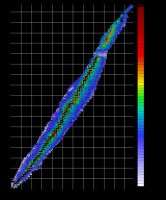
Распределение изотопов. По горизонтали – заряд ядра (число протонов). По вертикали – атомная масса (число нуклонов). Цвет – стабильность изотопа (продолжительность полураспада). Изотопы – нуклиды
ПОДРОБНЕЕ
Электронвольт
Электрон-вольт (обозначение: англ .- eV, укр .- эВ) – единица энергии. Энергию друг елеткрон-вольт приобретает один электрон, проходя через электростатический барьер с потенциалом один вольт. 1 эВ =
ПОДРОБНЕЕ
Ядро атома
Ядро – центральная часть атома. В ядре сосредоточены положительный электрический заряд и основная часть массы атома. По сравнению с размерами атома, который определяется радиусом электронных орбит,
ПОДРОБНЕЕ
Атомная энергия
Ядерная энергия (атомная энергия) – внутренняя энергия атомных ядер, выделяющаяся при некоторых ядерных превращениях. Использование ядерной энергии основано на осуществлении цепных реакций деления
ПОДРОБНЕЕ
Унунгексий
Унунгексий – (лат. Ununhexium, Uuh), эка-полоний – сто шестандцатую химический элемент VI группы периодической системы, атомный номер 116, атомная масса 293-й Временное обозначение – Uuh. История
ПОДРОБНЕЕ
Химический элемент
Химический элемент – тип (вид, сорт) атомов с одинаковым зарядом атомных ядер (т.е. одинаковым количеством протонов в ядре атома) и определенной совокупностью свойств, но масса ядра атома химического
ПОДРОБНЕЕ